生物医用纳米材料研发与测试
【研究目的】
癌症和心脑血管病变等是威胁人类健康的重大疾病,手术和化疗药物治疗等传统治疗方法具有根除不彻底和毒副作用大等不足。在开发的新兴治疗技术中,免疫治疗技术和纳米药物递送技术因其具有治愈率高、持续时间长、适用性广以及靶向输送效率高等优点,成为备受临床关注的研究热点。但是,鉴于人体结构的复杂型、疾病的多样性以及个体的差异性,新兴技术的研发尚存在特异性不足和药物递送效果不佳等难题。采用医工融合模式,创新性地开发具有高效药物递送效率的免疫治疗技术和纳米药物技术正面临着重大发展机遇。
【技术创新】
针对心血管疾病和癌症治疗中的药物递送靶组织不准,输送效率不高的问题,研究适用于免疫治疗和纳米药物治疗的载体材料。基于不同疾病的特异性和不同治疗方法的局限性,提出了具有针对性的纳米治疗策略,研发并制备了系列新型智能纳米材料,通过体内及体外实验验证其治疗效果。具体的创新点如下:
(1)肿瘤微环境响应纳米治疗:开发出由两亲性分子组装、加入了靶标分子和肿瘤微环境响应剂的智能纳米药物,实现了治疗药物在病灶组织的高效靶向富集,并能特异性地进行胞内高效可控的药物释放。实验证明其具有生物安全性和有效的肿瘤细胞杀伤能力;
(2)癌症免疫治疗:为克服肿瘤对单一治疗方法的耐药性,通过机器学习方法从小分子蛋白库筛选并设计出免疫检查点抑制剂,将其修饰在具有肿瘤组织归巢作用的载药外泌体上。外泌体释放化疗药物杀伤肿瘤组织,并通过脱落配体分子抑制免疫细胞的相关信号通路,改善肿瘤组织的免疫微环境,达到协同治疗的效果;
(3)动脉粥样硬化治疗:开发了靶向血管壁处胶原的多肽纳米药物,达到抑制血小板在血管壁处粘附的作用;设计了高效装载雷帕霉素的多肽纳米载体,以提高载药效率;构建了靶向斑块中氧化低密度脂蛋白的多肽纳米材料,从而实现将雷帕霉素从体液到斑块的精准递送,并进行了小型动物(小鼠)和中型动物(比格犬)体内实验,结果表明经过治疗后斑块面积明显减小,炎症因子浓度降低,说明多肽纳米材料能有效治疗动脉粥样硬化。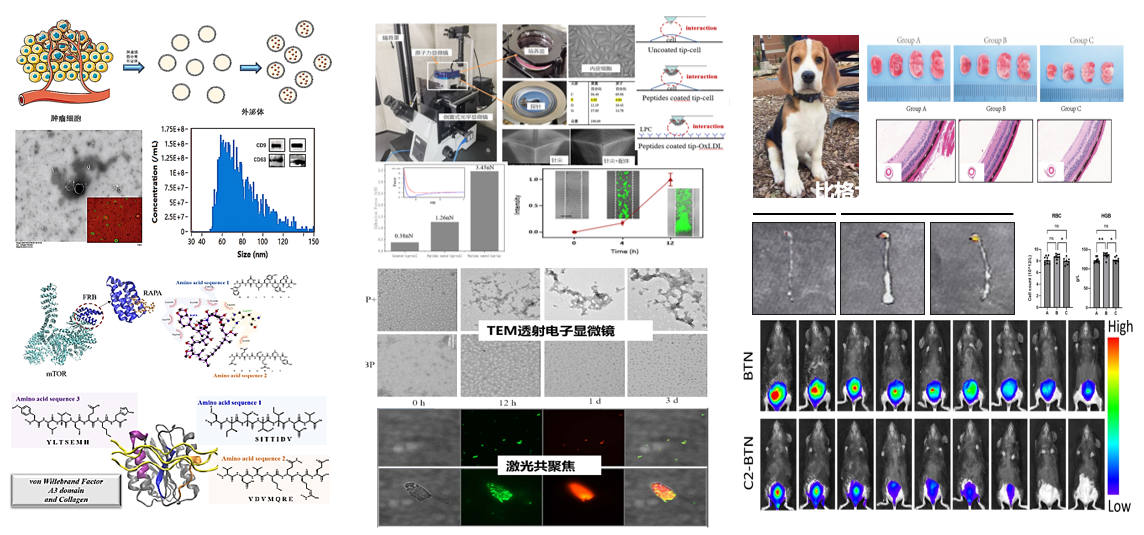
纳米材料设计生物界面相互作用测量动物活体实验和治疗效果评估
【知识产权】
发表相关研究论文20余篇;
授权发明专利5项。
【应用行业领域】
生物技术领域,医疗与健康领域,纳米材料领域等。
【成果应用情况】
2019-2023年,与国家科学纳米中心合作,开发了多种pH/配受体结合力响应下的多肽肿瘤药物;
2021-2022年,与清华大学合作,开发了用于化学动力学疗法的可促进肿瘤细胞内羟基自由基生成的铁/钯纳米催化剂;
2023年至今,与中国医学科学院分子肿瘤学国家重点实验室合作,开发针对食管鳞癌的外泌体载体药物。









